2025年3月1日に新しい採用ホームページを公開しました。 ● 新たな採用ホームページはこちら⇒(https://www.shionogi.com/jp/ja/recruit) ● 本ページに対応する新たなページはこちら⇒(https://www.shionogi.com/jp/ja/recruit/jobs/pharmacovigilance)
ファーマコビジランス職の仕事
どんな仕事?
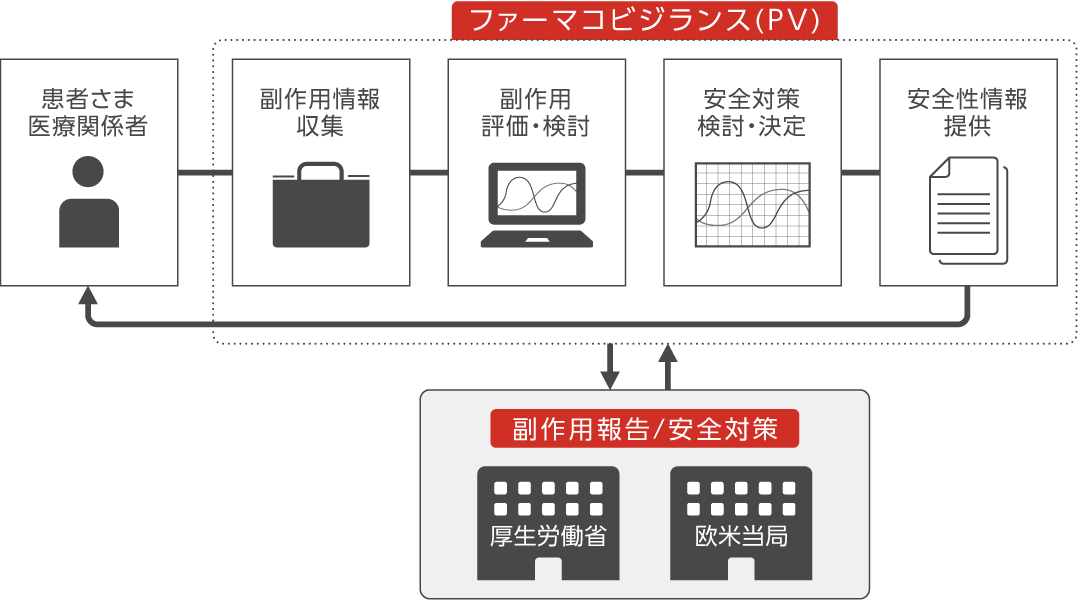
GVP(Good Vigilance Practice 安全管理の基準)、GPSP(Good Post-marketing Study Practice 製造販売後の調査及び試験の実施の基準)、その他の法規制遵守による高い信頼性を基盤として、開発から市販後までSHIONOGI製品の安全性に責任を持ち、安全性情報の収集・評価・分析・発信を行うことにより、社会のアンメットメディカルニーズにタイムリーに応える革新的で価値の高い製品の提供に貢献する仕事です。

どんな業務内容?
- 開発プロジェクトのメンバーとして、臨床試験の段階から開発品のリスクの特定と評価を行います
- 市販後の安全性情報の収集・評価・分析と規制当局への報告を行います
- 市販後のリスク管理計画を策定し、実行します
- 製造販売後調査を立案・実施して市販後の安全性・有効性を確認 し、適正使用のために有用な情報を提供します
- 集積された副作用を分析・評価し,Company Core Safety Information(CCSI)、Periodic Benefit Risk Evaluation Report(PBRER)等の各種文書の作成、添付文書の作成・改訂を行います
- 海外のSHIONOGIグループおよび関連会社と連携し、グローバルにSHIONOGI製品の安全性を評価します
- 日・米・欧・アジア地域におけるファーマコビジランス業務に係る規制を把握し対応します
- グローバルでのSHIONOGIグループのファーマコビジランス体制を維持・管理します
- ファーマコビジランス活動に関連するITシステムを企画・構築し運用します
取り組み事例
Head Quarterとして、全世界で実施される安全管理業務を取りまとめるなかで、現在はアジア、特に中国のPV(Pharmacovigilance、安全管理)体制構築に取り組んでいます。
- 中国におけるSHIONOGIのグループ会社である北京塩野義及び平安塩野義と密接に協力し、これらの企業における中国PV規制に準じたPV組織、体制作りを行っています。
- グループ会社だけではなく、販売や物流を実施する提携企業やPV業務を受託するベンダーとも連携しながら中国で発生した安全性情報を漏れなく適切に入手して安全性を評価するとともに、各国の規制当局に報告する仕組みを構築しています。
- 海外事業推進部、品質保証部及び薬事部等の社内関連部署と連携し、中国における様々な業務方針について協議・立案し、中国グループ会社や提携企業と協力しながら業務を遂行しています。
- 中国本土だけではなく、韓国、台湾等アジア各国のグループ会社や提携企業と連携し、各国からの安全性情報収集、安全性評価、当局報告等を実施しています。
- SHIONOGIが創製したCovid-19治療薬エンシトレルビル フマル酸をアジアやアフリカ等の中低所得国117カ国に広く提供することを目的として、国際的な公衆衛生機関であるMPPと協力し、世界中の国々から安全性情報を入手する仕組み作りを行っています。
デジタルトランスフォーメーション
ファーマコビジランスにおけるグローバルのヘッドオフィスとして、全世界の安全性情報を効率的に収集し、迅速な分析と適正使用情報の周知につなげるべく、ファーマコビジランスのデジタルトランスフォーメションに取り組んでいます。
- 安全性データベースをグローバルで統一し、情報処理プロセスを可能な限り自動化させるプロジェクト(タッチレスプロセッシングへのチャレンジ)を推進中です。
- 製品の問合せ窓口等に寄せられる膨大な情報から、NLP(自然言語処理)を用いて安全性情報を抽出する仕組みについて、アカデミアとの共同研究を実施中です。
- 電子調査票導入に関する業界への働きかけや、Webによる安全性情報収集など、情報収集に関するデジタライゼーションに力を入れています。
- 毎日入手する多数の安全性情報をミスなく迅速に処理するため、RPA(ロボティック・プロセス・オートメーション)やシステムを利用し、処理の自動化を進めています。
〒541-0045
大阪市中央区道修町3丁目1番8号
Copyright ©SHIONOGI & CO., LTD. All right reserved.


